新型双羟烷基季铵盐的合成与抗菌活性研究
时间:2015-05-15 18:30:56 来源: 点击量:
王春华* ;徐艳岩;孙居锋;侯桂革;刘文帅
(滨州医学院药学院,山东 烟台 264003)
摘要:以N-甲基二乙醇胺为原料合成了N-甲基-N-十四烷基-N,N-二羟乙基溴化铵和N-甲基-N-十六烷基-N,N-二羟乙基溴化铵两种双羟烷基基季铵盐(QAS)。采用红外光谱、核磁共振谱技术对所合成的化合物进行了结构了表征,并研究了其对金黄色葡萄球菌、枯草芽孢杆菌和大肠杆菌的抗菌性能。研究结果表明,在所研究的细菌种类范围内,两种季铵盐都具有良好的抗菌效果。
关键词:N-甲基二乙醇胺;合成;双羟基季铵盐;抗菌活性
Synthesis and antibacterial properties of novel quaternary ammonium salt with dihydroxy alkyl
WANG Chunhua; XU Yanyan; SUN Jufeng; Hou Guige; LIU Wenshuai
(School of Pharmacy, Binzhou Medical University, Yantai 264003, Shandong)
Abstract: Two quaternary ammonium salt bearing dihydroxy alkyl with antibacterial activity were synthesized using N-methyl diethanolamine (MDEA) and halogenated hydrocarbon (RX) as raw materials, namely N-methyl-N-tetradecyl-N,N-bis(2- hydroxyethyl) mmonium bromide, N-methyl-N-hexadecyl-N,N-bis(2- hydroxyethyl) ammonium bromide. Their structures were characterized by fourier transform infrared spectroscopy (FTIR) and nuclear magnetic resonance hydrogen spectrum (H-NMR); and their antibacterial properties against S. aureus, B.subtilis and E. coli were tested. The test results indicate that the two compounds have good antibacterial activity.
Keywords: N-methyl diethanolamine; Synthesis; Dihydroxy quaternary ammonium salts; Antibacterial activity
长链烷基季铵盐作为季铵盐类物质的一个主要品种,最大特点就是对物质有较强的吸附作用,通过这种吸附作用而在物质表面聚集成一层膜而具有柔软
[1]、抗静电、杀菌消毒
[2]、乳化等多种功能,在工业和民用上都有广泛的应用。对于小分子季铵盐抗菌剂的抗菌活性已经有了较多的研究 ,但是小分子抗菌剂存在易挥发、不易加工、 化学稳定性差等缺点
[3],而且应用时由于化学活性较低,基本以游离态存在,毒性相对较大,刺激性也强,将其作为抗菌剂应用在纺织品上是溶出型的,易洗脱,且易在人体表面逐渐富集,长期使用易产生病变。如果季铵盐分子中有活性基团,在使用时通过化学键键合在纤维表面,就能克服溶出型、易洗脱这一缺点,不会被人体汗液等分泌物吸收而进入人体形成生理障碍,对人体和环境具有很高的安全性;溶于醇或水,使用方便。由于长链烷基季铵盐基团具有很强的抗菌性能,因此本文合成了两种含有活性双羟基长链烷基季铵盐,并做了抑菌试验。结果表明,合成的两种季铵对研究范围内的几种细菌均有着不同程度的抑菌效果,既可以独立使用,也可以通过化学反应键合到其他材料中去。
1 实验部分
1.1仪器与试剂
红外光谱仪,Magna550 (Nicolet),KBr压片,测试范围400~4000cm
-1,分辨率4cm
-1,扫描次数32次。H
1NMR波谱仪BRUKER(av400),探头型号:5 mm DUL 13C-1,溶剂:DMSO。N-甲基二乙醇胺,分析纯,淄博市博山东方化工厂提供;十四烷基溴、十六烷基溴、N,N-二甲基甲酰胺,分析纯,均由天津金瑞特试剂有限公司提供。
1. 2 季铵盐的合成[4]
在250 ml三口烧瓶中,加入0.1 mol N-甲基二乙醇胺和50 ml N,N-二甲基甲酰胺,在电动搅拌下,用滴液漏斗向反应瓶中缓慢滴加0.1mol十二烷基溴,控制反应温度为80℃,反应8小时后加入100ml苯做沉淀剂。将得到的沉淀用无水乙醇反复重结晶得到产品N-甲基-N-十四烷基-N,N-二羟乙基溴化铵,产率64.5%。同样步骤合成N-甲基-N-十六烷基-N,N-二羟乙基溴化铵,反应温度70℃,反应时间10小时,产率56.7%。
1.3 抑菌性能测试
1.3.1 培养基的制备
(1)液体培养基的制备: 按照胰蛋白胨(Tryptone) 10 g/L、酵母提取物(Yeast extract) 5 g/L、氯化钠(NaCl) 10 g/L放入三角瓶中,加入蒸馏水配制好后调pH为7.4~7.6,加塞,高压蒸汽灭菌30 min备用。
(2)固体培养基的制备:按照营养琼脂33 g/L放入三角瓶中,加入蒸馏水配制好后加塞,高压蒸汽灭菌30 min,取出后趁热倒入培养皿中备用。
1.3.2 菌种活化
从低温冰箱(4 ℃)中取出菌斜面,用接种棒从菌斜面上取菌种,转移到液体培养基中,在37 ℃生化培养箱中培养14 h。
1.3.3 菌悬液的制备
用磷酸缓冲液稀释活化后的菌液使菌悬液的浓度约为1.0×10
9 cfu/mL,采用稀释平板计数法测活菌数。
1.3.4 抗菌测试方法[5]
季铵盐抗菌性能的测试分为定性测试方法—抑菌圈法和定量测试方法—振荡培养法,具体方法分别参考文献[6]与[7],以抑菌圈直径的大小作为评价季铵盐抑菌性能的依据,以抗菌率作为定量的依据。
抗菌率计算公式:
 2 结果与讨论
2.1化合物的结构表征
2.1.1 N-甲基-N-十四烷基-N,N-二羟乙基溴化铵
2 结果与讨论
2.1化合物的结构表征
2.1.1 N-甲基-N-十四烷基-N,N-二羟乙基溴化铵
IR(KBr):3289 cm
-1、1047 cm
-1处的强吸收峰分别为羟基和碳氧键的特征吸收峰;2920 cm
-1、2847 cm
-1的强吸收峰以及1467 cm
-1、1377cm
-1的吸收峰归属为亚甲基和甲基的特征吸收峰。在谱图中的指纹区域的723 cm
-1处出现了弱吸收峰,这一吸收峰的存在,表明在分子中存在直链烷基,即十四烷基
[8]。因此,红外光谱表明合成了N-甲基-N-十四烷基-N,N-二羟乙基溴化铵。
1H NMR(CD
3SOCD
3):δ=0.84~0.87(m,3H,C-CH
3),1.24~1.27(m,22H,11CH
2),1.66~1.67(m,2H,CH
2),3.09(s,3H,N-CH
3),3.35~3.41(m,2H,N-CH
2),3.44~3.45(m,4H,2N-CH
2),3.81~3.82(m,4H,2O-CH
2),5.23~5.26(m,2H,2OH)。重水交换后的5.23~5.26(m,2H,2OH)处吸收峰消失,其它峰不变,可证明化合物中两个羟基的存在。以上结果说明该化合物为N-甲基-N-十二烷基-N, N-二羟乙基溴化铵。
2.1.2 N-甲基-N-十六烷基-N,N-二羟乙基溴化铵
IR(KBr):3416 cm
-1、1043 cm
-1处的强吸收峰分别为羟基和碳氧键的特征吸收峰;2919 cm
-1、2850 cm
-1的强吸收峰以及1471 cm
-1、1385 cm
-1的吸收峰归属为亚甲基和甲基的特征吸收峰。在谱图中的指纹区域的721 cm
-1处出现了弱吸收峰,这一吸收峰的存在,表明在分子中存在直链烷基,即十六烷基
[8]。因此,红外光谱表明合成了N-甲基-N-十六烷基-N,N-二羟乙基溴化铵。
1H NMR(CD
3SOCD
3):δ=0.84~0.87(m,3H,C-CH
3),1.24~1.27(m,26H,13CH
2),1.65~1.67(m,2H,CH
2),3.08(s,3H,N-CH
3),3.34~3.38(m,2H,N-CH
2),3.43~3.44(m,4H,2N-CH
2),3.81~3.82(m,4H,2O-CH
2),5.23~5.26(m,2H,2OH)。重水交换后的5.23~5.26(m,2H,2OH)处吸收峰消失,其它峰不变,可证明化合物中两个羟基的存在。以上结果说明该化合物为N-甲基-N-十六烷基-N, N-二羟乙基溴化铵。
2.2 季铵盐抗菌性能研究
2.2.1 N-甲基-N-十四烷基-N,N-二羟乙基溴化铵
抗菌定性测试
N-甲基-N-十四烷基-N,N-二羟乙基溴化铵溶液对细菌的抑菌圈直径如表1所示。
表1 N-甲基-N-十四烷基-N,N-二羟乙基溴化铵的抑菌圈直径
Table 1 Diameter of inhibition zone of C14 QAS
| 样品(ppm) |
抑菌圈直径(mm) |
金黄色葡萄球菌
(S. aureus) |
枯草芽孢杆菌(B.subtilis) |
大肠杆菌
(E. coli) |
| 0 |
0 |
0 |
0 |
| 100 |
14.0 |
13.3 |
10.1 |
| 500 |
15.2 |
18.0 |
10.5 |
| 2500 |
16.7 |
21.1 |
11.2 |
由表1可知,N-甲基-N-十四烷基-N,N-二羟乙基溴化铵的浓度在100~2500 ppm范围对大肠杆菌、金黄色葡萄球菌和枯草芽孢杆菌时,滤纸片周围均有抑菌圈;并随其浓度的增加抑菌圈直径增大,且对枯草芽孢杆菌抑菌圈的直径在浓度500 ppm、2500 ppm时大于金黄色葡萄球菌和大肠杆菌的。说明N-甲基-N-十四烷基-N,N-二羟乙基溴化铵对大肠杆菌、金黄色葡萄球菌和枯草芽孢杆菌均具有抗菌效果,其中对枯草芽孢杆菌的抗菌效果最好。
抗菌定量测试
将不同浓度的N-甲基-N-十四烷基-N,N-二羟乙基溴化铵溶液与菌悬液在37 ℃下振荡3 h,其抗菌率的变化曲线如图1A所示。
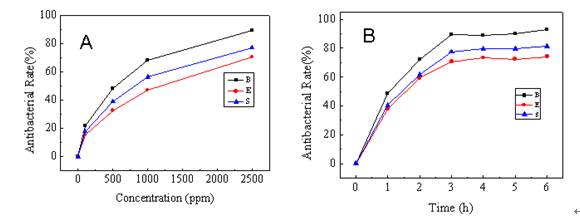 图1 A 和B分别为N-甲基-N-十四烷基-N,N-二羟乙基溴化铵在不同浓度、不同接触时间下的抗菌性
Figure 1 Antimicrobial activity of C14 QAS at different concentrations and
different contact times separately
图1 A 和B分别为N-甲基-N-十四烷基-N,N-二羟乙基溴化铵在不同浓度、不同接触时间下的抗菌性
Figure 1 Antimicrobial activity of C14 QAS at different concentrations and
different contact times separately
由图1A可见,N-甲基-N-十四烷基-N,N-二羟乙基溴化铵的抗菌率随着溶液浓度的增加而明显增大;在相同的浓度时,对枯草芽孢杆菌的抗菌率大于对金黄色葡萄球菌和大肠杆菌的。当浓度为2500 ppm时,对枯草芽孢杆菌的抗菌率达到89.57%,对金黄色葡萄球菌的为77.54%,对大肠杆菌的为70.69%。结果表明,N-甲基-N-十四烷基-N,N-二羟乙基溴化铵对大肠杆菌、金黄色葡萄球菌和枯草芽孢杆菌均具有良好的抗菌能力,其中对枯草芽孢杆菌的抗菌效果最好。
图1B为浓度是2500 ppm的N-甲基-N-十四烷基-N,N-二羟乙基溴化铵溶液在37℃振荡与菌悬液在不同接触时间下抗菌率的变化曲线。由图可见,短时间内(1~2 h)抗菌率迅速增大(即活菌数迅速下降),在接触3 h后,抗菌率基本达到最大值。说明N-甲基-N-十四烷基-N,N-二羟乙基溴化铵有较强的抗菌能力。
2.2.2 N-甲基-N-十六烷基-N,N-二羟乙基溴化铵 B
抗菌定性测试
N-甲基-N-十六烷基-N,N-二羟乙基溴化铵溶液对细菌的抑菌圈直径如表2所示。
表2 N-甲基-N-十六烷基-N,N-二羟乙基溴化铵的抑菌圈直径
Table 2 Diameter of inhibition zone of C16 QAS
| 样品(ppm) |
抑菌圈直径(mm) |
金黄色葡萄球菌
(S. aureus) |
枯草芽孢杆菌(B.subtilis) |
大肠杆菌
(E. coli) |
| 0 |
0 |
0 |
0 |
| 100 |
13.0 |
13.5 |
0 |
| 500 |
13.8 |
14.3 |
10.2 |
| 2500 |
14.6 |
15.5 |
10.6 |
由表2可知,N-甲基-N-十六烷基-N,N-二羟乙基溴化铵的浓度在100~2500 ppm对金黄色葡萄球菌和枯草芽孢杆菌时,滤纸片周围有抑菌圈;并随其浓度的增加抑菌圈直径增大,且对枯草芽孢杆菌抑菌圈的直径在各个浓度均大于金黄色葡萄球菌和大肠杆菌的;在100 ppm时对大肠杆菌滤纸片周围无抑菌圈,而在500 ppm、2500 ppm时稍有抑菌圈。说明N-甲基-N-十六烷基-N,N-二羟乙基溴化铵对大肠杆菌、金黄色葡萄球菌和枯草芽孢杆菌均具有一定的抗菌效果,其中对枯草芽孢杆菌的抗菌效果最好。
抗菌定量测试
将不同浓度的N-甲基-N-十六烷基-N,N-二羟乙基溴化铵溶液与菌悬液在37 ℃下振荡3 h,其抗菌率的曲线如图2C所示。
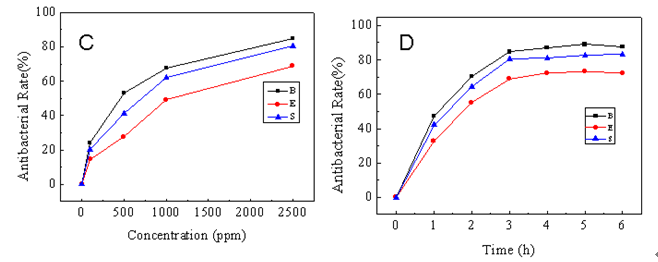 图2 C 和D分别为N-甲基-N-十六烷基-N,N-二羟乙基溴化铵在不同浓度、不同接触时间下的抗菌性
Figure 2 Antimicrobial activity of C16 QAS at different concentrations and
different contact times separately
图2 C 和D分别为N-甲基-N-十六烷基-N,N-二羟乙基溴化铵在不同浓度、不同接触时间下的抗菌性
Figure 2 Antimicrobial activity of C16 QAS at different concentrations and
different contact times separately
由图2C可见,N-甲基-N-十六烷基-N,N-二羟乙基溴化铵的抗菌率随着溶液浓度的增加而明显增大;在相同的浓度时,对枯草芽孢杆菌的抗菌率均大于对金黄色葡萄球菌和大肠杆菌的。当浓度为2500 ppm时,对枯草芽孢杆菌的抗菌率达到84.66%,对金黄色葡萄球菌的为80.43%,对大肠杆菌的为68.97%。结果表明,N-甲基-N-十六烷基-N,N-二羟乙基溴化铵对大肠杆菌、金黄色葡萄球菌和枯草芽孢杆菌均具有良好的抗菌能力,其中对枯草芽孢杆菌的抗菌效果最好。
图2D为浓度是2500 ppm的N-甲基-N-十六烷基-N,N-二羟乙基溴化铵溶液在37 ℃振荡与菌悬液在不同接触时间下抗菌率的变化曲线。由图可见,短时间内(1~2 h)抗菌率迅速增大(即活菌数迅速下降),在接触3 h后,抗菌率基本达到最大值。说明N-甲基-N-十六烷基-N,N-二羟乙基溴化铵有较强的抗菌能力。
3 结论
以N-甲基二乙醇胺为原料合成了N-甲基-N-十四烷基-N,N-二羟乙基溴化铵和N-甲基-N-十六烷基-N,N-二羟乙基溴化铵三种双羟烷基季铵盐。两种双羟烷基季铵盐对大肠杆菌、金黄色葡萄球菌和枯草芽孢杆菌均具有一定的抗菌能力,且抗菌率随着溶液浓度的增加而明显增大。当浓度为2500 ppm时,两种季铵盐对枯草芽孢杆菌的抗菌率分别达到89.57%、84.66%,对金黄色葡萄球菌的分别为77.54%、80.43%,对大肠杆菌的分别为70.69%、68.97%。
参考文献
[1]崔淑玲, (赵立环。 A季铵盐在纺织品加工中的应用[J]。印染助剂,2006,23(4):7-9。
[2]王伟平,杨建洲3-十六烷氧基-2-羟基丙基三甲基氯化铵的合成及性质研究[J]。应用化工,2008,37(10):1206-1209。
[3]佟会,邱树毅。季铵盐类抗菌剂及其应用研究进展[J]。贵州化工,2006,31(5):1-6。
[4]张学同,周贵忠,廖双泉。N,N-二甲基乙醇胺三个季铵盐衍生物的合成与表征[J]。合成化学, 2002,(5):451-453。
[5]J金永安,姜生。纺织品抗菌性能检测方法及其评估[J]。北京纺织,2005,26(1):49-51。
[6]李方,弓太生,曹云红。鞋用抗菌剂及其制品抗菌效力的评价方法[J]。 中国皮革, 2007,36(1):46-49。
[7]孟春丽。纺织品的抗菌防臭整理技术[J]。河南纺织高等专科学校学报,2004,16(3):61-64。
[8] 邓芹英,刘岚, 邓慧敏。 波谱分析教程[M]。北京:科学出版社, 2003:45-46。


